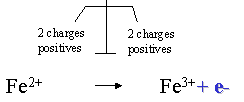R�action d'oxydor�duction: pond�ration d'�quations
I. M�thode pas à pas de pond�ration d'une �quation d'oxydor�duction
Pour pond�rer une �quation d'oxydor�duction, il faut utiliser une m�thode particulière.
Elle va comporter 12 �tapes qui permettent d'arriver à la pond�ration correcte. Au fil des exercices, certaines �tapes vous para�tront superflues, mais pour d�buter, voici un modèle de r�solution qui pourra être bien utile !
I. Dissocier en ions les acides forts, les bases fortes et les sels, laisser les autres compos�s sous forme mol�culaire :
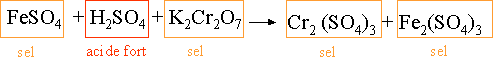
![]()
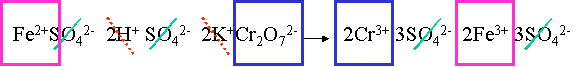
II. Simplifier les ions inchang�s dans les deux membres même s'ils ne sont pas en même quantit�. Mettre entre parenthèses les �l�ments qui n'apparaissent que dans un membre :
![]()
III. Identifier les couples :
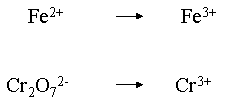
IV. D�terminer l'�tage d'oxydation des �l�ments :
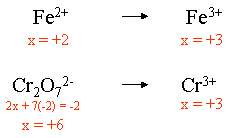
V. �change d'�lectrons à partir de l'�tage d'oxydation :
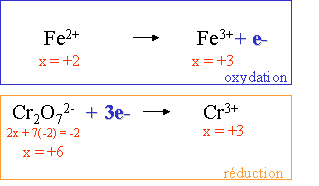
VI. V�rification du nombre d'�l�ments mis en r�action et pond�ration �ventuelle :
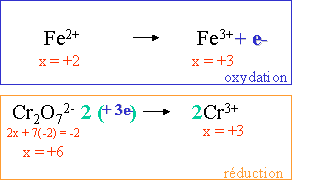
VII. �quilibrage des charges gr�ce au milieu (ajout de H+ en milieu acide et de OH- en milieu basique):
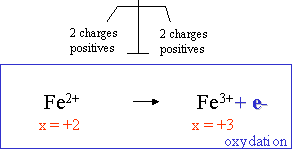 |
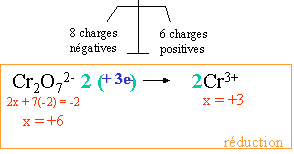 |
|
|
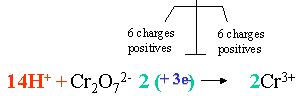 |
VIII. �quilibrage des masses ; il faut qu'il y ait le même nombre d'atomes dans chaque membre, or l'on a rajout� 14H+ d'un c�t�. Ceux-ci s'associeront à l'oxygène de Cr2O72- pour former 7 mol�cules d'H2O.
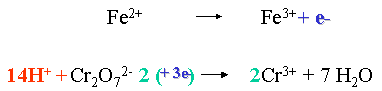
IX. Bilan : il faut que le nombre d'�lectrons �chang�s au cours de la r�action soit �gal, il faut donc multiplier l'une des deux �quations voire les deux.
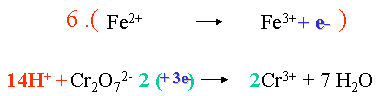
X. Addition membre à membre :
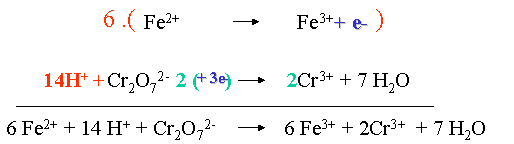
XI. R��criture de l'�quation sous forme mol�culaire, en regardant de quels compos�s proviennent les �l�ments.
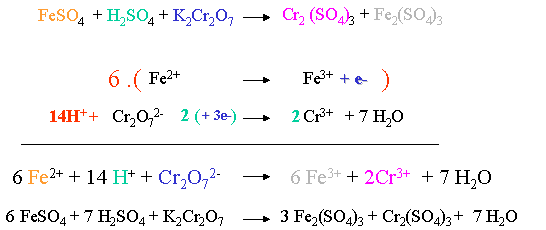
XII. V�rification de la pr�sence en même quantit� de mêmes �l�ments de part et d'autre de l'�quation (principe de Lavoisier), simplifier si possible les mol�cules d'eau :
Il manque 2 K+ et un SO42- dans le membre de droite. L'on doit donc y rajouter K2SO4.
XIII. L'�quation pond�r�e est :
![]()
Synthèse :
| 1.Dissocier en ions les acides forts, les bases fortes et les sels, laisser les autres compos�s sous forme mol�culaire. |
| 2. Simplifier les ions inchang�s dans les deux membres même s'ils ne sont pas en même quantit�s. Mettre entre parenthèses les �l�ments qui n'apparaissent que dans un membre. |
| 3. Identifier les couples. |
| 4. D�terminer l'�tage d'oxydation des �l�ments. |
| 5. �change d'�lectrons à partir de l'�tage d'oxydation. |
| 6. V�rification du nombre d'�l�ments mis en r�action et pond�ration �ventuelle. |
| 7. �quilibrage des charges gr�ce au milieu (ajout de H+ en milieu acide et de OH- en milieu basique). |
| 8. �quilibrage des masses ; il faut qu'il y ait le même nombre d'atomes dans chaque membre. |
| 9. Bilan : il faut que le nombre d'�lectrons �chang�s au cours de la r�action soit �gal, il faut donc multiplier l'une des deux �quations voire les deux. |
| 10. Addition membre à membre. |
| 11. R��criture de l'�quation sous forme mol�culaire, en regardant de quels compos�s proviennent les �l�ments. |
| 12. V�rification de la pr�sence en même quantit� de mêmes �l�ments de part et d'autre de l'�quation (principe de Lavoisier), simplifier si possible les mol�cules d'eau : |
![]() Attention,
si l'une des �tapes ne fonctionne pas, c'est qu'une erreur s'est gliss�e dans
le parcours. Ainsi le nombre de H+ ou de OH- ajout� doit
toujours pouvoir former un nombre entier de mol�cules d'eau dans l'autre membre
(sauf si des �l�ments H et O sont d�jà pr�sents dans les deux membres,
ils doivent toutefois être pr�sents en même quantit� dans chaque
membre, principe de Lavoisier).
Attention,
si l'une des �tapes ne fonctionne pas, c'est qu'une erreur s'est gliss�e dans
le parcours. Ainsi le nombre de H+ ou de OH- ajout� doit
toujours pouvoir former un nombre entier de mol�cules d'eau dans l'autre membre
(sauf si des �l�ments H et O sont d�jà pr�sents dans les deux membres,
ils doivent toutefois être pr�sents en même quantit� dans chaque
membre, principe de Lavoisier).
|
Copyright (c) 2000 - 2020 | Miseur Ludovic | www.lachimie.net | tous droits r�serv�s | remis � jour le : 21/10/2020 |
|
|
|
Comment citer cette page : |
| Miseur, L. (2020). Lachimie.net - pond�ration d'�quations d'oxydor�duction. La Chimie.net. http://www.lachimie.net | |
|
|