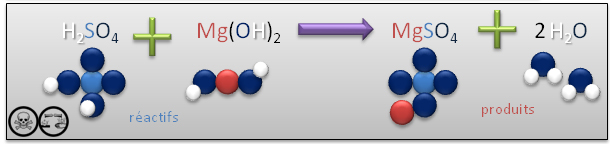
Les fonctions chimiques
I. Formules et fonction
I.1. La formule g�n�rale
R�gles et conventions pour d�terminer la formule g�n�rale d'un compos� chimique au d�part de sa formule mol�culaire.
Conventions
- on remplace les symboles des �l�ments m�talliques (ou � pr�dominance m�tallique) par le symbole g�n�ral M;
- on remplace les symboles des �l�ments non-m�talliques (ou � pr�dominance non-m�tallique) par le symbole g�n�ral X;
- on conserve les symboles de l'oxyg�ne O et de l'hydrog�ne H;
- on supprime les indices et les parenth�ses.
De la sorte, nous obtenons les formules g�n�rales d'un nombre limit� de corps purs compos�s:
| Formule mol�culaire | Formule g�n�rale | Formule mol�culaire | Formule g�n�rale |
| HNO3 | HXO | Fe2O3 | MO |
| Al2(SO4)3 | MXO | H2S | HX |
| NaCl | MX | KOH | MOH |
| CO2 | XO | H2SO4 | HXO |
| CuO | MO | N2O3 | XO |
| Mg(OH)2 | MOH | AgNO3 | MXO |
On constate qu'il n'y a que 7 cat�gories de corps purs compos�s dont les formules g�n�rales sont: HXO, MXO, MX, XO, MO, MOH et HX.
I.2. Les fonctions chimiques
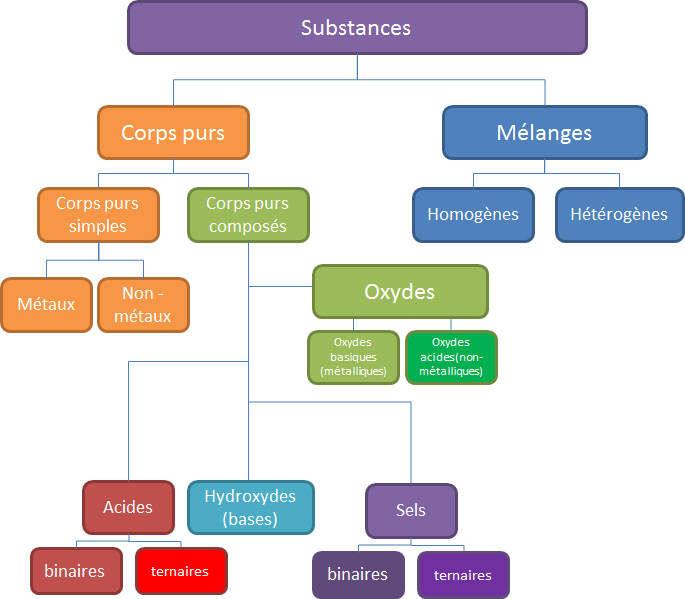
La mati�re qui nous entoure peut �tre class�e selon plusieurs crit�res, un premier classement s�pare les corps purs des m�langes. Un corps purs est une mati�re compos�e de mol�cules identiques ayant toutes la m�me propri�t� que cette mati�re � l'�chelle atomique.
Un second classement peut s'op�rer au point de vue de la composition chimique des mol�cules qui composent se corps purs. Selon le type d'atomes et la r�activit� chimique (la fa�on dont r�agissent les corps purs) d'autres grandes classification de la mati�re peuvent �tre faites au d�part des corps purs.
Formule g�n�rale Nom de la formule g�n�rale (nom de la fonction chimique) Exemple MO Oxyde m�tallique Fe2O3 XO Oxyde non-m�tallique CO2 MOH Hydroxyde (base hydroxyl�e) Ca(OH)2 HX Acide binaire (hydracide) HCl HXO Acide ternaire (oxacide) H3PO4 MX Sel binaire (sel d'hydracide) KCl MXO Sel ternaire (sel d'oxacide) Al2(SO4)3 soit 4 grandes fonctions (cat�gories):
Oxydes:
MO et XOHydroxydes ou bases hydroxyl�es:
MOHAcides:
HX et HXOSels:
MX et MXO
II. Caract�ristiques des diff�rentes fonctions
II.1. Les Oxydes non-m�talliques
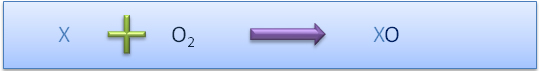
Formule g�n�rale : XO
Un oxyde non-m�tallique est le r�sultat de la combustion d'un non-m�tal (corps pur simple). C'est � dire, sa r�action avec du dioxyg�ne (O2).
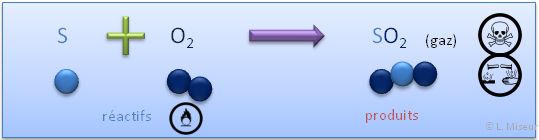
Exemple : Combustion du soufre dans le dioxyg�ne
R�action :
Obtention : r�action d'un non-m�tal avec le dioxyg�ne
Quelques oxydes non-m�talliques et leurs utilisations :
- N2O : protoxyde d'azote : "gaz hilarant", utilis� comme anesth�siant
- CO2 : dioxyde de carbone : � -78�C, il se pr�sente sous forme d'un solide blanc, c'est la glace carbonique.
- CO : monoxyde de carbone : gaz inodore et incolore qui est produit lors de mauvaise combustion. Il est extr�mement toxique et cause chaque ann�e des centaines de d�c�s.
II.2. Oxyde m�tallique
Formule g�n�rale : MO
Un oxyde m�tallique est le produit de la r�action de combustion d'un m�tal avec le dioxyg�ne.
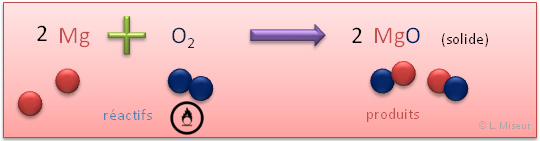
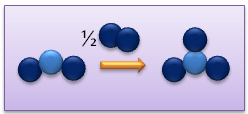
Exemple : Combustion du magn�sium dans le dioxyg�ne
R�action :
Obtention : r�action d'un m�tal avec le dioxyg�ne
Quelques oxydes m�talliques et leurs utilisations :
- MgO : Oxyde de magn�sium : utilis� sous forme de briques dans les fours industriels. L'oxyde de magn�sium est un mat�riau r�fractaire.
- PbO : Oxyde de plomb (II) : utilis� comme �lectrode dans les accumulateurs au plomb.
- Al2O3 : Oxyde d'aluminium : minerai (source naturelle) d'aluminium. Ce minerai est appel� Bauxite
- Cr2O3 : Oxyde de Chrome (III) : source naturelle (minerai) de chrome.
- Fe2O3 : Oxyde de Fer (III) : source naturelle (minerai) de fer. Ce minerai est appel� H�matite.
II.3. Hydroxyde (base hydroxyl�e)
Formule g�n�rale : MOH
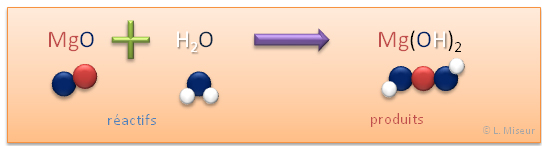
Exemple : r�action de l'oxyde de magn�sium avec l'eau
Obtention : r�action d'un oxyde m�tallique avec l'eau.
Le compos� form� est un hydroxyde ou base hydroxyl�. Il a est basique. Les hydroxydes sont des bases.
Les bases peuvent �tre caract�ris�es selon les crit�res suivants :
Les bases sont caustiques, ont une saveur amère et bleuissent le tournesol.
Les bases peuvent �tre d�tect�es en utilisant des indicateurs.
Un indicateur est une substance qui change de couleur selon le milieu dans lequel elle se trouve. Ainsi, les indicateurs permettent selon leur couleur de d�tecter si une substance est plut�t basique ou plut�t acide.
Voici quelques indicateurs et les couleurs qu'ils prennent en pr�sence d'acide ou de base :
Quelques autres indicateurs acide-base
Quelques hydroxydes et leurs utilisations :
- Mg(OH)2 : Hydroxyde de magn�sium aussi appel� lait de magn�sium est utilis� comme antiacide pour l'estomac
- NaOH : Hydroxyde de sodium appel� couramment soude caustique est utilis� comme d�boucheur (Destop�)
- KOH : Hydroxyde de potassium appel� aussi soude potassique est utilis� en biologie.
- Al(OH)3 : Hydroxyde d'aluminium : anti-transpirant, d�odorant.
> Attention ! Les hydroxydes sont caustiques et br�lent la peau en s'attaquant � une des prot�ines (mol�cule particuli�re) qui la compose.
II.4. Acide binaire (hydracide)
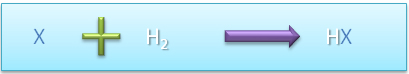
Formule g�n�rale : HX
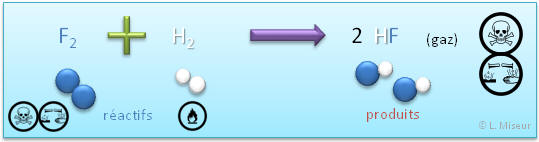
Exemple : r�action du difluor avec le dihydrog�ne
Cette r�action permet de produire du fluorure d'hydrog�ne (acide fluorhydrique) utilis� afin de graver le verre. (Cette substance est l'une des rares qui attaque le verre. Elle est utilis�e dans la gravure sur verre)
Protocole de gravure sur verre (Par Saint-Just) - http://www.saint-gobain-glass.com/saint-just/
DESCRIPTION
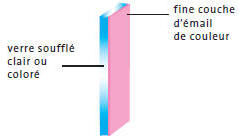
La gravure � l�acide est une des m�thodes de gravure (il existe �galement le sablage). C�est un enl�vement de mati�re par voie chimique. Elle fait appara�tre le verre sous
des aspects diff�rents (transparent, d�poli ou d�grad�).
A/ PR�PARATION
1) Nettoyer le verre support face �mail avec de l��thanol
(cf Photo n�1).
2) Poser votre pochoir sur la couche d��mail (cf Photo n�2).
3) Laisser uniquement la zone � graver apparente. Pour
cela, utiliser du vinyle ou du scotch : faire un r�servoir ou butyl pour �viter la dispersion de l�acide (cf photo 3)
B/ GRAVURE
4) Remplir le b�cher en t�flon d�acide fluorhydrique �
40%. En verser de petites quantit�s sur la surface �
graver. (cf Photo n�4).
5) �taler l�acide fluorhydrique � l�aide d�un pinceau jusqu�� l�obtention du rendu souhait�. Rajouter de l�acide fluorhydrique si n�cessaire (cf Photo n�5)
C/ RIN�AGE
6) Rincer � l�eau abondamment (cf Photo n�6)
7) Retirer le scotch et le pochoir (cf Photo n�7).
A noter : le temps de gravure peut varier fortement en fonction de la taille du motif � graver et du type de lettrage (d�tails), de la quantit� de mati�re active, de l��paisseur de la couche d��mail et la teinte de base. Il conviendra donc d�int�grer ces points dans le temps de pr�paration des projets. Le rendu varie selon la dilution en % de la dilution aqueuse de l�acide, le temps d�exposition et l��paisseur de la couche d��mail. Pour les verres opales et s�l�nium, renouveler r�guli�rement l�acide (car saturation rapide).T�l�charger la fiche technique explicative
Obtention : r�action d'un �l�ment non-m�tallique avec le dihydrog�ne
Le compos� form� est un acide binaire. C'est un acide.
Les acides peuvent �tre caract�ris�s selon les crit�res suivants :
Les acides ont une saveur aigre, rougissent le papier indicateur (tournesol) et r�agissent avec les bases pour former des sels. Quelques acides binaires et leurs utilisations :
- HF : Fluorure d'hydrog�ne : gravure sur verre
- HCl : Chlorure d'hydrog�ne : utilis� dans la production des mati�res plastiques, utilis� �galement comme d�tartrant et comme d�capant.
- HBr : Bromure d'hydrog�ne : utilis� en chimie organique (synth�se et catalyseur).
II.5. Acide ternaire (oxacide)
Formule g�n�rale : HXO
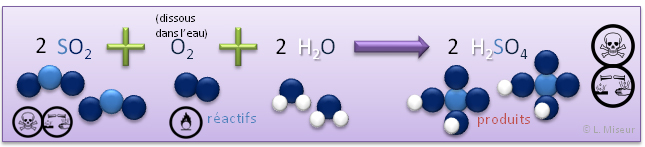
Exemple 1: r�action du dioxyde de soufre avec l'eau (en pr�sence d'oxyg�ne)
L'acide sulfurique peut �tre produit au d�part de dioxyde de soufre, toutefois, le dioxyde de soufre devra d'abord r�agir avec le dioxyg�ne pour former du trioxyde de soufre, qui lui r�agit avec l'eau pour former l'acide sulfurique (sulfate d'hydrog�ne).
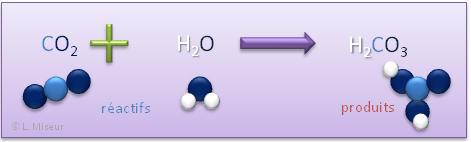
Exemple 2 : r�action du dioxyde de carbone avec l'eau
C'est ce ph�nom�ne qui est � l'origine des grottes. En effet, l'eau de pluie se charge en dioxyde de carbone et devient acide. Cette acidit� attaque le calcaire et creuse des grottes.
Obtention : r�action d'un oxyde non-m�tallique avec l'eau
Quelques acides ternaires et leurs utilisations :
- H2SO4 : Sulfate d'hydrog�ne (acide sulfurique) : utilis� dans les accumulateurs et composant des pluies acides.
- H3PO4 : Phosphate d'hydrog�ne (acide phosphorique) : acidifiant, pr�sent notamment dans le Coca-Cola.
- HNO3 : Nitrate d'hydrog�ne (acide nitrique) : intervient dans la fabrication des engrais azot�s. M�lang� au chlorure d'hydrog�ne il forme l'eau r�gale, un acide puissant capable de dissoudre l'or.
II.6. Sel binaire (sel d'hydracide)
Formule g�n�rale : MX
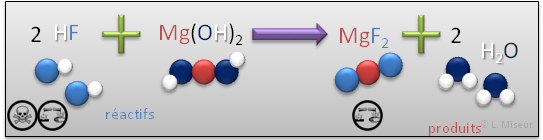
Exemple: r�action du fluorure d'hydrog�ne avec l'hydroxyde de magn�sium
Obtention : r�action d'un acide binaire avec un hydroxyde
Quelques sels binaires et leurs utilisations :
- NaCl : Chlorure de sodium : sel de cuisine.
- CaCl2 : Chlorure de calcium : sel de d�neigement.
- CaF2 : Fluorure de calcium : cristal de fluorine utilis� en bijouterie :
- MgCl2 : Chlorure de Magn�sium : permet de coaguler le lait de soja pour la fabrication du tofu.�
SiCl4 : Chlorure de silicium : nuage artificiel.
CrCl3: Chlorure de chrome (III) : traitement imperm�abilisant des textiles.
II.7. Sel ternaire (sel d'oxacide)
Formule g�n�rale : MXO
Exemple: r�action du sulfate d'hydrog�ne avec l'hydroxyde de magn�sium
Obtention : r�action d'un acide ternaire avec un hydroxyde
Quelques sels ternaires et leurs utilisations :
- MgSO4 : Sulfate de magn�sium (Sels d'Epson) : utilis� comme laxatif.
- Na2CO3 : Bicarbonate de soude : utilis� comme antiacide pour l'estomac ou anti-odeur.
- PbCrO4 : Chromate de plomb : pigment jaune (marquage de travaux sur autoroute). (toxique)
- PbSO4 : Sulfate de plomb : pigment jaune (toxique).
- BiVO4 : Vanadate de bismuth : pigment jaune (substitut non toxique)
III. Tableau de synth�se des diff�rentes fonctions
Compl�te le tableau ...
Formule g�n�rale Nom de la formule g�n�rale (nom de la fonction chimique) Formation / type de r�activit� Exemple X + O -> XO P2O5 M + O -> MO Na2O MO + H2O ->MOH LiOH X + H2 -> XH H Br XO + H2O -> HXO HNO3
MOH + HX -> MX + H2O PbCl2 MOH + HXO -> MXO + H2O
Ba3( PO4 )2
IV.Exercices



R�serv� à une utilisation strictement priv�e-tous droits de reproduction et de diffusion r�serv�s - (c) L. Miseur - La chimie.net 2010
Copyright (c) 2000 - 2020 | Miseur Ludovic | www.lachimie.net | tous droits r�serv�s | remis � jour le : 21/10/2020
Comment citer cette page : Miseur, L. (2020). Lachimie.net - Les fonctions chimiques. La Chimie.net. http://www.lachimie.net