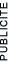Les mol�cules
I. Mod�lisation des mol�cules
La mati�re est faite de mol�cules, compos�es d'atomes, mais comment repr�senter ces mol�cules ?

De nombreuses fa�ons de repr�senter les mol�cules existent. L'une d'elle est de repr�senter simplement les mol�cules par des boules color�es et une variante est de repr�senter les atomes qui constituent la mol�cule en r�alisant un assemblage de boules color�es, chaque boule repr�sentant alors un atome.
 |
 |
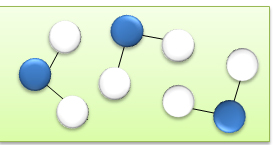 |
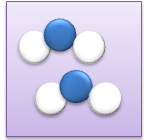
| Repr�sentation des mol�cules d'eau sous forme de boules bleues | Repr�sentation des mol�cules d'eau mettant en �vidence sa composition atomique (2 hydrog�nes (blanc) et 1 oxyg�ne (bleu)) | Repr�sentation des mol�cules d'eau mettant en �vidence sa composition atomique (2 hydrog�nes (blanc) et 1 oxyg�ne (bleu)) et la forme moyenne de la mol�cule |
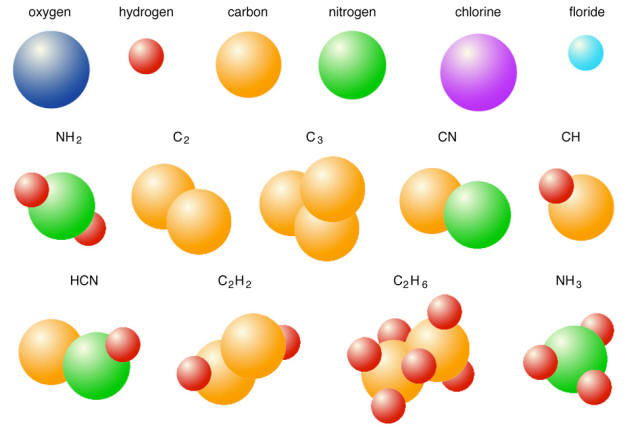
Repr�sentation de mol�cules mettant en �vidence la composition atomique et l�gende
Ces repr�sentations permettent de mettre en �vidence certaines caract�ristiques des mol�cules mais n'est vraiment pas commode. La premi�re repr�sentation sous forme de boules est la moins pr�cise, elle ne permet pas de mettre en �vidence la composition de la mol�cule, ni sa g�om�trie. De plus les mol�cules ne ressemblent pas � des petites boules !
Observons l'image d'une mol�cule r�alis�e par IBM avec un microscope � effet tunnel :
|
Mol�cule correspondant � l'assemblement de 8 atomes de c�sium et 8 atomes d'iode (c) Hopkinson, Lutz & Eigler -Cesium & Iodine on Copper (111) | http://www.almaden.ibm.com/vis/stm/hexagone.html |
Nous voyons bien que cette mol�cule n'est pas une sph�re ! Elle semble plut�t lin�aire.
Notre fa�on de repr�senter les mol�cules sous formes de boules color�es ou m�me d'un assemblage de boules color�es n'est donc pas la plus ad�quate. Elle devient surtout fastidieuse lorsque nous devons �crire les mol�cules dans un texte ou r�soudre des �quations chimiques.
... Sans oublier les probl�mes li�s � l'utilisation des couleurs (daltoniens...), la d�finition d'une l�gende universelle, ...
II. Formules mol�culaires
Pour repr�senter facilement les mol�cules, les chimistes ont pr�f�r�s laisser de c�t� les probl�mes de formes et de g�om�tries et ont d�cid�s d'utiliser une �criture SYMBOLIQUE.
Pour symboliser une mol�cule, on utilise les symboles des atomes, ceux-ci ordonn�s selon des conventions et mettant en �vidence la composition des mol�cules gr�ce � des coefficients et des indices.
|
|
|
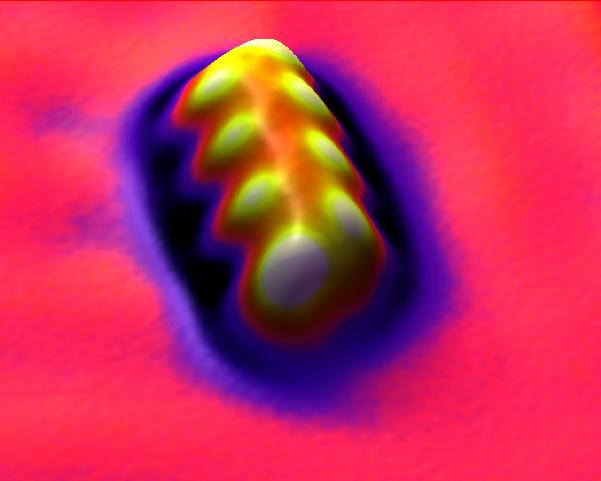
pour repr�senter une mol�cule, nous utilisons une formule chimique (ex: H2SO4 : une mol�cule de sulfate d'hydrog�ne) en orange, devant la mol�cule , c'est le coefficient , il se distribue sur tous les atomes qui forment la mol�cule en blanc, rouge et bleu, c'est les atomes (symboles) Hydrog�ne, Soufre et Oxyg�ne en vert et mauve, c'est l'indice , celui-ci multiplie l'atome qu'il pr�c�de (Il y a donc 4 atomes d'oxyg�ne par mol�cule) |
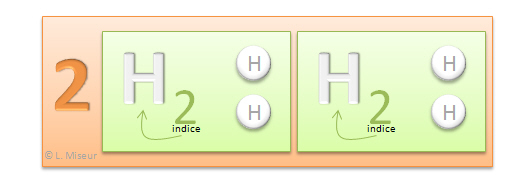
Nombre d'atomes : 2.2 H = 4 atomes d'H (hydrog�ne)
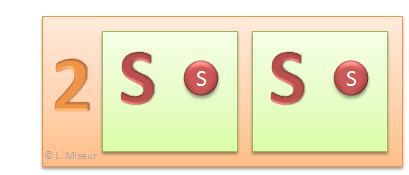
2.1 S = 2 atomes de S (soufre)
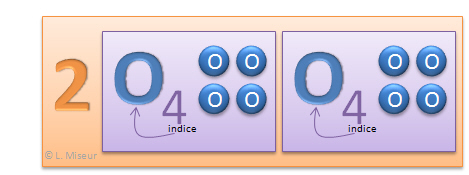
2.4 O = 8 atomes d'O (oxyg�ne)
Nombre de mol�cules : 2 (c'est le coefficient devant la mol�cule)
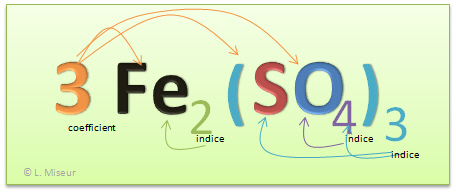
Dans l'exemple donn�, il n'y a pas que deux �l�ments diff�rents qui composent cette mol�cule, il y en a trois. SO4 est en fait un groupement, c'est � dire une mini mol�cule qui se comporte comme si il ne s'agissait que d'un atome lorsque l'on construit la mol�cule sur papier. Ce groupement peut aussi �tre soumis � l'effet d'un indice, dans ce cas, le groupement est mis entre parenth�ses et l'indice se note en dessous de la parenth�se. Exemple : Fe2(SO4)3
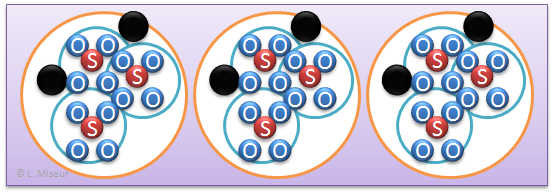
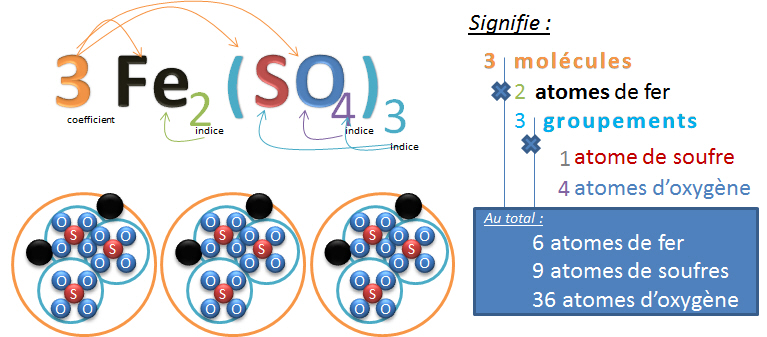
Quelques illustrations
(extraites du site de J. Thonnard - www.proftnj.com)
| �criture chimique (SYMBOLISME) | repr�sentation (selon le mod�le des boules) | signification |
| Cl |
|
1 atome non li� |
| 2 Cl |
|
2 atomes non li�s |
| Cl2 |
|
1 mol�cule (avec 2 atomes li�s) |
| 2 Cl2 |
|
2 mol�cules (avec 2 atomes li�s par mol�cule) |
| 4 Cl |
|
4 atomes non li�s |
| 4 Cl2 |
|
4 mol�cules (avec 2 atomes li�s par mol�cule) |
| �criture chimique | nombre total d'atomes diff�rents |
| 2 O3 | 6 O |
| Fe2O3 | 2 Fe, 3 O |
| Mg(OH)2 | 1 Mg, 2 O, 2 H |
| Cu(NO3)2 | 1 Cu, 2 N, 6 O |
| 2 K3Co(NO2)6 | 6 K, 2 Co, 12 N, 24 O |
| 2 mol�cules contenant chacune 3 atomes d'oxyg�ne | 2 O3 |
| 1 mol�cule contenant 1 atome de magn�sium et 2 groupements contenant chacun 1 atome d'oxyg�ne et 1 atome d'hydrog�ne | Mg(OH)2 |
| 3 mol�cules contenant chacune 2 atomes d'aluminium et 3 groupements contenant chacun 1 atome de soufre et 4 atomes d'oxyg�ne | 3 Al2(SO4)3 |
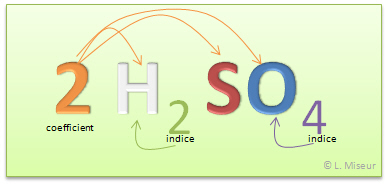
Construire des mol�cules
 | |
R�serv� � une utilisation strictement priv�e-tous droits de reproduction et de diffusion r�serv�s - (c) L. Miseur - La chimie.net 2010 | |
|
Copyright (c) 2000 - 2020 | Miseur Ludovic | www.lachimie.net | tous droits r�serv�s | remis � jour le : 21/10/2020 |
|
|
|
Comment citer cette page : |
| Miseur, L. (2020). Lachimie.net - Mol�cules. La Chimie.net. http://www.lachimie.net | |
|
|